Je ne comprends pas comment une réaction peut être d'ordre 1 si l'unité de k n'est pas en temps^-1.
Dans ce qcm je suis d'accord qu'il s'agit d'un ordre 1 (pour les memes raisons que la correction), mais j'aurais dit que k est faux car l'unité ne devrait être ni en mol.L^-1.s ni en mol.L^-1.min^-1
Parmi les propositions suivantes, choisir la (les) proposition(s) exacte(s) :
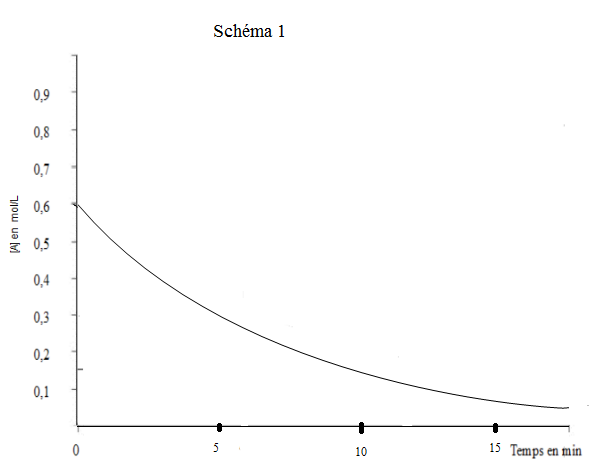
On considère la réaction suivante : A→B+C
A. La vitesse instantanée de la réaction à t=0 est de : 8×10−2mol.L−1.s
B. Pour calculer la vitesse instantanée il faut connaitre l'ordre de la réaction.
C. On peut déterminer l'ordre de la réaction grâce au schéma 1.
D. L'ordre de la réaction est 2
E. L'ordre de la réaction est 1
A. FAUX. On peut bien entendu calculer la pente de la tangente à la courbe à t=0 mais si on regarde l'unité de la vitesse, on constate tout de suite qu'elle est fausse. Elle est même presque doublement fausse ! Explications... (z'avez vu le suspens ? :p)
D'abord, l'unité de temps : dans l'énoncé elle est en seconde alors que sur le schéma elle est en min (j'espère donc que tous ceux qui ont calculé la tangente ont pensé à faire la conversion même si j'espère que personne n'a calculé la tangente pour la raison qui suit)
La vitesse s'exprime en concentration.temps−1 donc en mol.L−1.s−1 ou en mol.L−1.min−1 donc l'unité était de toute façon fausse
B. FAUX. Pas du tout, il suffit de tracer la tangente à la courbe au point souhaité, l'ordre de la réaction n'intervient pas dans la détermination de la vitesse instantanée.
C. VRAI. On constate que la courbe est une exponentielle décroissante, de plus t1/2 est indépendant de la concentration de A. En effet on peut observer que l'intervalle de temps durant lequel la concentration a diminué de moitié est indépendant de la concentration de A. Ceci est caractéristique de l'ordre 1 !
D. FAUX. Cf réponse C.
E. VRAI. Cf réponse C
Merci d'avance!
